妇科肿瘤的治疗正经历着前所未有的变革,随着分子生物学和精准医学的突破,新一代药物不仅为患者带来更长的生存期,也在治疗安全性上实现了重要优化。从基因突变到免疫微环境,科学家们通过“生物标志物导航”为每位患者量身定制方案,而新型药物技术的出现,正将曾经的“绝症”推向慢性病管理的可能。(以下内容基于最新临床研究进展,为不同治疗阶段的患者提供实用指导。)
一、精准打击:靶向治疗的三大突破方向
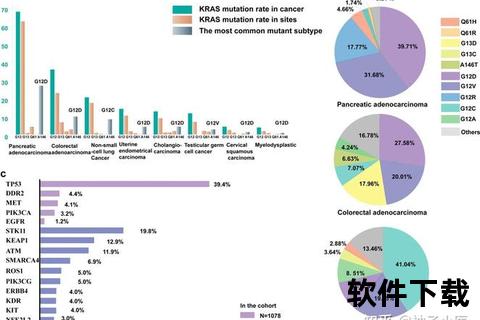
1. 基因缺陷的精准修复
约15%-20%的卵巢癌患者携带BRCA基因突变,这类患者对PARP抑制剂(如帕米帕利)敏感。通过“合成致死”机制,药物选择性杀伤癌细胞,而对正常细胞影响较小。BRIGHT研究显示,BRCA突变患者使用帕米帕利联合贝伐珠单抗的中位无进展生存期(PFS)达6个月,客观缓解率(ORR)28.6%。但需注意,长期使用可能产生耐药性,需定期监测血液学毒性。
2. 肿瘤微环境的免疫调控
CD8+肿瘤浸润淋巴细胞(TILs)水平是预测免疫治疗疗效的关键指标。BRIGHT研究中,CD8+TILs≥3的铂耐药卵巢癌患者接受替雷利珠单抗联合化疗后,ORR提升至48.6%,中位总生存期(OS)达17.9个月。对于免疫治疗无效的患者,可考虑联合抗血管生成药物(如贝伐珠单抗),通过改善肿瘤血管通透性增强药物渗透。
3. 新型药物载体的精准投送
抗体药物偶联物(ADC)结合了靶向性和化疗药物的杀伤力。针对Nectin-4的ADC药物9MW2821在宫颈癌临床试验中,客观缓解率(ORR)达40.5%,疾病控制率(DCR)89.2%,且对经铂类化疗和免疫治疗失败的患者仍有效。这类药物需警惕中性粒细胞减少等血液毒性,治疗期间需每周监测血常规。
二、安全优化:从“有效”到“可控”的临床策略
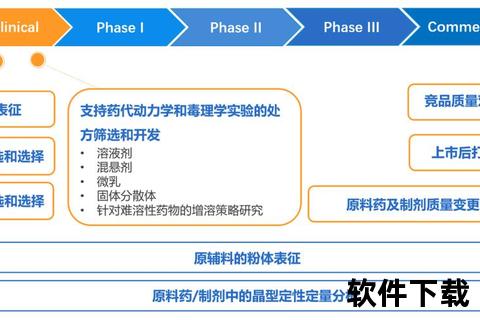
1. 分子分型指导下的分层治疗
2. 不良反应的主动管理
3. 特殊人群的个体化方案
三、患者行动指南:从诊断到康复的关键决策
1. 诊断阶段的主动参与
2. 治疗过程中的自我管理
3. 复发预警与就医时机
四、未来展望:从实验室到床旁的转化机遇
液体活检技术(如ctDNA监测)可提前3-6个月预测耐药;人工智能模型(如OncoCast)能整合基因组、临床特征推荐最优方案。患者可通过参与临床试验(如NCT05044871)获得前沿治疗,但需充分知情超说明书用药风险。
疾病的复杂性要求医患共同决策:在追求疗效的平衡生活质量。正如BRIGHT研究所启示的,生物标志物不仅是治疗的路标,更是打开个体化医疗之门的钥匙。(本文涉及治疗方案需在专业医生指导下实施。)




